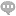2014年,NobuyukiHanamura等在PersonalizedMedicine上发表了《GlobaldevelopmentstrategyforcompaniondiagnosticsbasedontheusageandapprovalhistoryforbiomarkersinJapan,theUSAandtheEU》,总结了伴随诊断的开发策略,以及伴随诊断全球开发过程中面临的主要挑战[7],上海一体化伴随诊断郑重承诺。如图4所示,伴随诊断开发策略主要有四种方式:1.策略一:如果药物开发(DrugDevelopment)初期,用于患者筛选(PatientSelection)的生物标志物(Biomarker,BM)是明确的,临床试验应该对生物标志物阳性(BiomarkerPositiveCohorts)、阴性(BiomarkerNegativeCohorts)的两个队列进行研究,并且有已经获批的体外诊断(InVitroDiagnostic,IVD)用于该生物标志物的检测时,上海一体化伴随诊断郑重承诺,上海一体化伴随诊断郑重承诺,那么应该采用共同开发(Co-development)的策略。共同开发的伴随诊断举例:①CrizotinibandtheVysisALKBreakApartFISHkit(Japan,USA)②CetuximabandEGFRPharmDx(Japan,USA)③PanitumumabandEGFRPharmDx(Japan,USA)④PanitumumabandtheTheraScreenKRASmutationkit。 方法简单易行,医保覆盖,适于临床推广。上海一体化伴随诊断郑重承诺
发挥吉因加自主品牌测序平台在性能、应用、合规和数据安全方面的优势,共同推动‘因人而异’**精细***的临床落地和推广应用。信达生物是一家覆盖***药物领域的国内***创新型药企,相信双方通过此次通力合作,可以共推FGFR2突变胆管*患者的精细***,让更多患者受益。”2020年4月17日,FDA批准pemigatinib(PemazyreTM)用于***既往接受过***的携带FGFR2融合或重排的局部晚期或转移性胆管*患者,pemigatinib是***个也是***一个被FDA批准用于此适应症的***药物。胆管*恶性程度高预后差,目前已有的系统***对不能手术切除或晚期胆管*疗效较差,二线及以上的***更是缺乏有效的***药物和方案。FDA批准pemigatinib主要基于一项在美国开展的FIGHT-202研究结果。在携带FGFR2基因融合或重排的患者(队列A)中,pemigatinib单药***的总体缓解率为36%(主要终点),中位DOR为(次要终点)。pemigatinib已于2019年2月获得FDA授予的“突破性疗法认定”,用于***复发且存在FGFR2基因易位的晚期/转移性或不可手术切除的胆管*患者;并于2018年3月获FDA授予的孤儿药认定,用于***胆管*患者。关于Pemigatinibpemigatinib(PemazyreTM)由信达生物合作伙伴Incyte研发。浙江伴随诊断试剂盒迈杰转化医学具备从样本制备到H&E,IHC、FISH、RNAscope及多重免疫组化等全套组织病理和分子病理检测能力。
2.策略二:当没有批准的IVD用于该生物标志物的检测时,应该使用实验室自建检测(Laboratory-DevelopedTests,LDTs)进行患者筛选,如果药物开发后期有IVD获批,应该进行桥接研究(BridgingStudy)验证LDT与IVD具有非常类似的检测性能(VerySimilarPerformanceCharacteristics)。例如曲妥珠单抗在乳腺*临床试验时使用临床试验检测(ClinicalTrialAssay,CTA)进行患者筛选,后来通过桥接研究证明了HercepTest与CTA检测结果的一致性。3.策略三:如果药物开发初期,用于患者筛选的生物标志物不明确,临床试验不需要进行基于生物标志物分组的队列研究。一旦生物标志物明确,应该进行回顾性分析(RetrospectiveAnalysis)来评价生物标志物。如果生物标志物阳性队列的有效性或安全性(Efficacy/Safety)优于阴性队列,那么药物说明书(DrugLabel)中应该增加生物标志物的相关信息。例如KRASmutationkits和其伴随药物西妥昔单抗(Cetuximab),就是通过这种策略开发的。
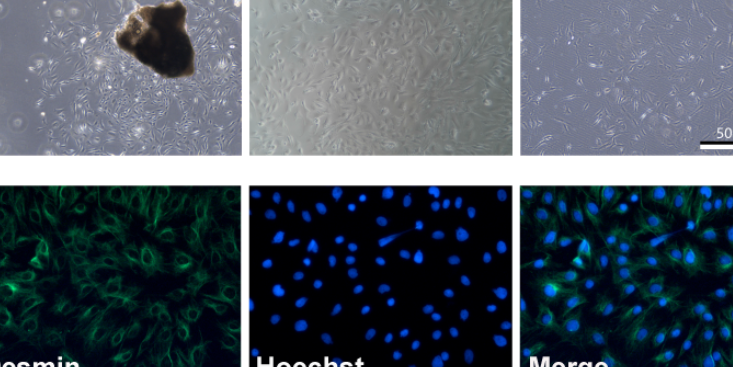
伴随诊断(companiondiagnostic,CD)是一种体外诊断技术,能够提供有关患者针对特定***药物的***反应的信息,有助于确定能够从某一***产品中获益的患者群体,从而改善***预后并降低保健开支。此外,伴随诊断还有助于确定**有可能针对***药物产生响应的患者群体。伴随诊断提供的信息对于安全有效地使用相应的***产品(药品或生物制品)至关重要。伴随诊断是帮助临床医生找到带有特定靶位变化的患者,在提高靶向药物疗效、***安全性以及降低医疗成本方面发挥关键作用,是实现**精细医疗的基石。迈杰转化医学利用新一代智能技术补充传统医学的检测模式,赋能医疗健康建设,更好地为临床和患者服务。
以PCR平台为首的院内伴随诊断市场,一大多小的格局已形成,艾德生物占据细分市场**地位。目前伴随诊断伴随主要在医院病理科开展,伴随诊断试剂通过招标进院,艾德生物以其先发优势占据将近70%的市场份额。NGS通量高、精确率高,但检测成本高,高通量检测对临床的指导意义有待进一步挖掘,短时间内很难替代PCR的应用,NGS在临床上普遍是以LDT(LaboratoryDevelopedTests)形式,把样品送到院外的第三方检测,并向患者直接收费。主要原因是大多数医院没有大规模开展NGS的条件,缺人才、缺设备。如果NGS的成本进一步下降至价格不敏感的位置,很有可能成为主流的检测方式。据MarketsandMarkets数据,2016年全球伴随诊断市场规模约19亿美元左右,到2018年预计31亿美元,2016年至2022年的年复合增长率预计达到22.78%,显着高于全球IVD整体行业6%的增长速度。目前中国市场规模约3亿美元。过去7年,中国CAGR超30%,且有加速趋势。迈杰转化医学建立了符合质量体系规定的覆盖全平台的伴随诊断产品研发实验室、质检实验室,拥有GSP证书。上海一体化伴随诊断郑重承诺
迈杰转化医学目前已完成约30+靶点的方法学验证,50+靶点的方法学建立。上海一体化伴随诊断郑重承诺
荧光PCR技术是目前临床基因检测的优先方案,因其精确、快速、简单且成本较低,荧光PCR仪一次反应可以容纳96个或者384个样品,检测通量要高于FISH、IHC等技术;在除了高通量测序以外的技术中,荧光PCR也是检测DNA变异类型**多的方法。此外,荧光PCR法技术壁垒较低,易于生产。荧光PCR的弱点也很明显,由于原理所限,荧光PCR法只能检测常见位点的突变,无法覆盖该基因的所有碱基,这可能导致忽略某些稀有的突变得到假阴性的结果,从而造成误判。FISH技术目前只用于检测基因扩增和融合基因,结果可直接在显微镜下观察到,过程直观操作简单,是产品数量*次于荧光PCR的方法。这种方法的局限性在于只适用于检测单个基因片段的融合或扩增。并且需要较为专业的判读技术。二代测序技术的出现为**的易感基因检测、伴随诊断、个性化用药等提供了更佳的技术支撑和选择,尤其是基于NGS的aizhengpanel检测使得该领域检测可以更加快速和低廉,达到了同时检测若干个基因和突变位点的目的。上海一体化伴随诊断郑重承诺
文章来源地址: http://yyby.shopjgsb.chanpin818.com/swzp/swzdsj/deta_15151217.html
免责声明: 本页面所展现的信息及其他相关推荐信息,均来源于其对应的用户,本网对此不承担任何保证责任。如涉及作品内容、 版权和其他问题,请及时与本网联系,我们将核实后进行删除,本网站对此声明具有最终解释权。




 [VIP第1年] 指数:3
[VIP第1年] 指数:3